![]()
私たちの体内では、新陳代謝の過程や放射線などによって、活性酸素やフリーラジカルがつくられています。これらによって、細胞や細胞で一番重要な染色体内のDNAも損傷を受けます。しかし、私たちにはこの損傷を修復してくれる機能が備わっています。
一度に大量の放射線を受けると、この修復力を超えるため、骨髄や内臓などの機能が低下し、最悪の場合、死にいたることもあります。しかし、放射線の量が少ないときは、DNAにできた傷はほとんど修復されます。まれにDNAの傷が修復されないで残存しても、p53遺伝子がつくるp53タンパクが細胞内の自爆装置のスイッチを押して、この傷をもった不良細胞は自爆(アポトーシス)して人体組織から排除されます。このような防衛機構のおかげで、私たちの身体は少しの放射線にはびくともしないようにできているのです。
原爆放射線約1.5シーベルトを胎内で被ばくして生まれた子供の手、足、顔などの異常の頻度に増加は見られませんでした。1.5シーベルトのガンマ線をマウスの妊娠中期に瞬時に照射すると奇形が多発します。すなわち、放射線による発生異常に対しては、人はマウスより放射線に対する防衛機能が高いといえます。
妊娠中期のマウスにガンマ線を2シーベルト瞬時に照射すると、奇形が約60%も発生しました。しかし、同じ量を少しずつ27時間かけて照射した場合は、奇形の頻度は10%に減り、被ばくしない場合と比較して有意の差がなくなりました。
放射線による致命的な傷はDNAの2本鎖の切断で、これは、「非相同末端結合修復」と「組換え修復」で修復されます。前者は短時間で修復作業が完了しますが、2本鎖切断の一部しか修復しません。残りは組換え修復の作業ですが、この修復作業には時間がかかります。したがって、放射線による傷が少しずつできるときは、最初の傷が組換え修復で修復が完了してから次の傷ができれば、この傷も修復が完了するでしょう。しかし、瞬時の照射では、修復できない傷がたくさん残存します。ガンマ線の瞬時の照射では奇形が多発し、少しずつの照射では奇形リスクがゼロになったのは、2本鎖切断の修復効率が少しずつの照射では向上するからだと考えられます。図1に組換え修復の模型を示します。(ここで述べるマウス実験の原著:Kato et al, Inc J Radiat Biol 77,13,2001)
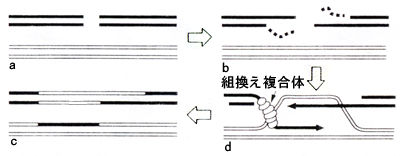
| 図1 組換え修復の模型 | |
|
|
|
以上は、p53遺伝子を持っているp53(+/+)マウスの場合です。p53遺伝子を欠損したp53(-/-)マウスでは、2シーベルトのガンマ線を少しずつ27時間かけて照射した場合でも、奇形の頻度は30%もあって、ガンマ線を照射しない場合の頻度18%より有意に高いままでした。この結果は次のように解釈できます。放射線によるDNAの傷は少しずつの照射の場合でも、修復されない傷が残存します。p53遺伝子をもっているマウスでは、p53タンパクが残存する傷を探知して細胞の自爆装置のスイッチを押すので、不良細胞は自爆(アポトーシス)して排除されます。したがって、放射線による害が完治するのです。しかし、p53(-/-)マウスにはp53タンパクがないので、アポトーシスが働きません。したがって、放射線によるDNAの傷が残存して、これが奇形の原因になるのです。ガンマ線の照射中に調べたところ、p53(+/+)マウスでは、アポトーシスの活性が盛んでしたが、p53(-/-)マウスではアポトーシスの活性はゼロでした。
以上の実験結果から、 放射線への少しずつの被ばくの場合は、放射線によるDNAの傷に対する「効率よく働くDNA修復」と、「活発なアポトーシス」の共同作業のおかげで、放射線によるDNAの傷は完全に組織から排除される、といえるでしょう。
原爆放射線を1シーベルト被ばくした小児の白血病頻度は、被ばくしない場合の21倍です(バックグランド分が1で、増加分が20)。リスクが被ばく量に直線比例するなら、50ミリシーベルトのリスクは、被ばくしない場合の2倍なります(バックグランド分が1で、増加分が1)。しかし、チェルノブイリ事故の放射線降下物で高濃度に汚染したベラルーシ国のゴメリの小児たちは、5年間で約50ミリシーベルト被ばくしたのに、白血病頻度はチェルノブイリ事故の前と後で同じです。放射線降下物による放射線は毎年10ミリシーベルトの汚染であったので、小児の身体は、このような少しずつの放射線による白血病のリスクにはびくともしなかったのです。
マウスに放射性水素(トリチウム)を含む水を生涯にわたって飲ませると、一年間の被ばく量が20シーベルトでは、リンパ腫瘍が20%と多発しますが、1年間の被ばく量が0.3シーベルト以下になるとリンパ腫瘍のリスクはゼロになります。
老化の主因は活性酸素だろうといわれています。活性酸素によってDNAの構成要素である塩基が損傷を受け、DNAの一本鎖切断も自然に多発しています(表1)。長い間、DNAの2本鎖切断は、放射線でしかできない傷であるとして、これが放射線が特別にこわい原因であると信じられていました。しかし、最近、組換え修復のときに働くRad51遺伝子(図1cの説明参照)を欠損したマウスの卵は、受精後数日で全部死亡することが発見されました。この原因は、分裂細胞にはDNAの2本鎖切断が自然に多発し、Rad51遺伝子欠損の細胞では組換え修復不全となり、細胞が全部死んでしまうからです。すなわち、放射線でできるDNAの傷は、全て自然にも発生しているのです。したがって、放射線は独特のDNA損傷をおこすものとして、特別にこわがらねばならない科学的根拠はなくなりました。では、どの程度の被ばくまでなら、放射線は安全でしょうか? 表1にこの疑問に対する答えの資料を用意しました。

| 表1 | DNAの損傷の種類と量:自然によるものとX線やガンマ線によるものの比較 |
DNA2本鎖切断は、自然に毎日細胞1個あたりに約10個発生していると推定されます。放射線を自然放射線の平均の強さの365倍受けるとすると、毎日1ミリシーベルトになり、この程度の被ばくによる2本鎖切断は表1から毎日0.03個で、自然の傷の0.3%です。この程度なら、自然の傷の治癒機能の範囲内で私たちの身体はびくともしないでしょう。
(引用資料の原著は近藤宗平:「人は放射線になぜ弱いか」
講談社ブルーバックス(1998)に譲る)